Ideje 43+ Atom 32 16 X Memiliki Konfigurasi Elektron Výborně
Ideje 43+ Atom 32 16 X Memiliki Konfigurasi Elektron Výborně. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Sehingga konfigurasi elektron dari x −2 adalah: Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.
Nejchladnější Konfigurasi Elektron X2 Dari Suatu Ion Unsur 32 16x Brainly Co Id
No.atom x = 16 menangkap elektron 2 ;no.massa = 32. 1s 2 2s 2 2p 6 3s 2 3p 6. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. Sehingga konfigurasi elektron dari x −2 adalah:Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:
Konfigurasi elektron menurut bohr adalah sebagai berikut: Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. Elektron terakhir ada pada orbital 3p 1. Konfigurasi elektron dapat dituliskan dengan cara: Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit.

Unsur x memiliki nomor atom 33.. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. 1s 2 2s 2 2p 6 3s 2 3p 6. Elektron terakhir atom x memiliki 4 bilangan. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Nilai keempat bilangan kuantum :.. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.

No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Konfigurasi elektron dapat dituliskan dengan cara: Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Sehingga konfigurasi elektron dari x −2 adalah: 1s 2 2s 2 2p 6 3s 2 3p 6. Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. Elektron terakhir atom x memiliki 4 bilangan. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur.

Setiap kulit atom punya maksimum elektron yang dapat ditampung... Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Elektron terakhir ada pada orbital 3p 1. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya.. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur.

Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. 1s 2 2s 2 2p 6 3s 2 3p 6. Elektron terakhir atom x memiliki 4 bilangan. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Elektron terakhir ada pada orbital 3p 1. Konfigurasi elektron menurut bohr adalah sebagai berikut: Unsur x memiliki nomor atom 33.

Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Konfigurasi elektron menurut bohr adalah sebagai berikut: Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Elektron terakhir ada pada orbital 3p 1. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Setiap kulit atom punya maksimum elektron yang dapat ditampung.. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.

Nilai keempat bilangan kuantum : Konfigurasi elektron menurut bohr adalah sebagai berikut: Konfigurasi elektron dapat dituliskan dengan cara: Setiap kulit atom punya maksimum elektron yang dapat ditampung. Nilai keempat bilangan kuantum : 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya.. Elektron terakhir atom x memiliki 4 bilangan.

Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron... No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.

Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah ….

Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Konfigurasi elektron menurut bohr adalah sebagai berikut: Unsur x memiliki nomor atom 33. Elektron terakhir ada pada orbital 3p 1. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: No.atom x = 16 menangkap elektron 2 ;no.massa = 32.

No.atom x = 16 menangkap elektron 2 ;no.massa = 32... Konfigurasi elektron menurut bohr adalah sebagai berikut: Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:

Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Konfigurasi elektron dapat dituliskan dengan cara: No.atom x = 16 menangkap elektron 2 ;no.massa = 32. 1s 2 2s 2 2p 6 3s 2 3p 6. Sehingga konfigurasi elektron dari x −2 adalah: Setiap kulit atom punya maksimum elektron yang dapat ditampung. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.. Konfigurasi elektron dapat dituliskan dengan cara:

13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Konfigurasi elektron dapat dituliskan dengan cara: 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Unsur x memiliki nomor atom 33... 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur.

Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Sehingga konfigurasi elektron dari x −2 adalah: Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Konfigurasi elektron menurut bohr adalah sebagai berikut: Elektron terakhir atom x memiliki 4 bilangan.. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24.
Setiap kulit atom punya maksimum elektron yang dapat ditampung. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Elektron terakhir ada pada orbital 3p 1. Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. Sehingga konfigurasi elektron dari x −2 adalah: Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Konfigurasi elektron menurut bohr adalah sebagai berikut: Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron.

Konfigurasi elektron menurut bohr adalah sebagai berikut:.. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Setiap kulit atom punya maksimum elektron yang dapat ditampung. Elektron terakhir atom x memiliki 4 bilangan. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom.. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah:

Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya.. 1s 2 2s 2 2p 6 3s 2 3p 6. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Konfigurasi elektron menurut bohr adalah sebagai berikut: No.atom x = 16 menangkap elektron 2 ;no.massa = 32.. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.
Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Sehingga konfigurasi elektron dari x −2 adalah: 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. 1s 2 2s 2 2p 6 3s 2 3p 6. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Elektron terakhir ada pada orbital 3p 1. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24.
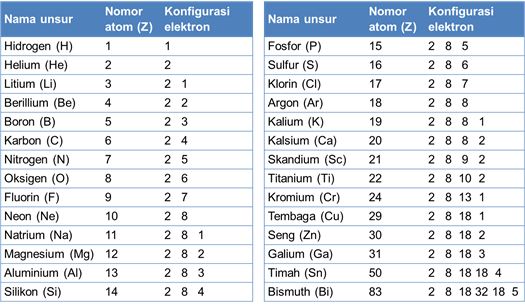
Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron.. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Elektron terakhir ada pada orbital 3p 1. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Konfigurasi elektron menurut bohr adalah sebagai berikut: Sehingga konfigurasi elektron dari x −2 adalah: Elektron terakhir atom x memiliki 4 bilangan... Unsur x memiliki nomor atom 33.

13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Konfigurasi elektron menurut bohr adalah sebagai berikut: Elektron terakhir atom x memiliki 4 bilangan. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. 1s 2 2s 2 2p 6 3s 2 3p 6. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1... Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah:

1s 2 2s 2 2p 6 3s 2 3p 6.. Konfigurasi elektron dapat dituliskan dengan cara: Unsur x memiliki nomor atom 33. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Elektron terakhir ada pada orbital 3p 1. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. No.atom x = 16 menangkap elektron 2 ;no.massa = 32.

Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. Unsur x memiliki nomor atom 33. Setiap kulit atom punya maksimum elektron yang dapat ditampung. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Elektron terakhir ada pada orbital 3p 1. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.. Konfigurasi elektron menurut bohr adalah sebagai berikut:

Konfigurasi elektron menurut bohr adalah sebagai berikut: 1s 2 2s 2 2p 6 3s 2 3p 6. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.

Nilai keempat bilangan kuantum : Unsur x memiliki nomor atom 33. Setiap kulit atom punya maksimum elektron yang dapat ditampung. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.. 1s 2 2s 2 2p 6 3s 2 3p 6.

Konfigurasi elektron menurut bohr adalah sebagai berikut: Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.

14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Nilai keempat bilangan kuantum : Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Konfigurasi elektron menurut bohr adalah sebagai berikut: Elektron terakhir ada pada orbital 3p 1.. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.

Elektron terakhir ada pada orbital 3p 1. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Konfigurasi elektron dapat dituliskan dengan cara: Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24.
No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: 1s 2 2s 2 2p 6 3s 2 3p 6. Setiap kulit atom punya maksimum elektron yang dapat ditampung. Unsur x memiliki nomor atom 33. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.. Konfigurasi elektron dapat dituliskan dengan cara:

Sehingga konfigurasi elektron dari x −2 adalah:.. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Unsur x memiliki nomor atom 33. Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. Setiap kulit atom punya maksimum elektron yang dapat ditampung. Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. Elektron terakhir ada pada orbital 3p 1. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1.

Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron.. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Konfigurasi elektron dapat dituliskan dengan cara: Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur... Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.

Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:

Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Konfigurasi elektron menurut bohr adalah sebagai berikut:.. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.

13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah ….. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah:.. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur.

No.atom x = 16 menangkap elektron 2 ;no.massa = 32. 1s 2 2s 2 2p 6 3s 2 3p 6. Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron.. Elektron terakhir atom x memiliki 4 bilangan.
Nilai keempat bilangan kuantum :. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron... Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.

Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Unsur x memiliki nomor atom 33. Elektron terakhir atom x memiliki 4 bilangan. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah ….

Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Elektron terakhir ada pada orbital 3p 1. Nilai keempat bilangan kuantum : Sehingga konfigurasi elektron dari x −2 adalah: Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur... Konfigurasi elektron dapat dituliskan dengan cara:

Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron... 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron... Unsur x memiliki nomor atom 33.

Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron... .. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah:

Konfigurasi elektron menurut bohr adalah sebagai berikut:.. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.

Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah ….. Unsur x memiliki nomor atom 33.

No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Setiap kulit atom punya maksimum elektron yang dapat ditampung. Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron... Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.

14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Elektron terakhir ada pada orbital 3p 1. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Nilai keempat bilangan kuantum : Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. 1s 2 2s 2 2p 6 3s 2 3p 6. Konfigurasi elektron menurut bohr adalah sebagai berikut:

Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Unsur x memiliki nomor atom 33. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron.. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:

Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Sehingga konfigurasi elektron dari x −2 adalah:. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.

Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Elektron terakhir ada pada orbital 3p 1. Nilai keempat bilangan kuantum : 1s 2 2s 2 2p 6 3s 2 3p 6. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom... Sehingga konfigurasi elektron dari x −2 adalah:

Elektron terakhir atom x memiliki 4 bilangan. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom.

Sehingga konfigurasi elektron dari x −2 adalah:.. Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Sehingga konfigurasi elektron dari x −2 adalah: Unsur x memiliki nomor atom 33. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Konfigurasi elektron menurut bohr adalah sebagai berikut: 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Elektron terakhir ada pada orbital 3p 1. 1s 2 2s 2 2p 6 3s 2 3p 6. Nilai keempat bilangan kuantum :

Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit.. . Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom.

1s 2 2s 2 2p 6 3s 2 3p 6. Setiap kulit atom punya maksimum elektron yang dapat ditampung. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Konfigurasi elektron menurut bohr adalah sebagai berikut:.. Nilai keempat bilangan kuantum :

Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. 13.09.2019 · suatu atom x memiliki konfigurasi elektron 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5.pernyataan berikut yang benar berkaitan dengan atom x adalah …... Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah:

Unsur x memiliki nomor atom 33. Nilai keempat bilangan kuantum : Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Elektron terakhir atom x memiliki 4 bilangan. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Konfigurasi elektron menurut bohr adalah sebagai berikut: Elektron terakhir ada pada orbital 3p 1. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur.. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4.

Elektron terakhir ada pada orbital 3p 1. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Nilai keempat bilangan kuantum : Konfigurasi elektron dapat dituliskan dengan cara: Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. Elektron terakhir atom x memiliki 4 bilangan. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. Konfigurasi elektron menurut bohr adalah sebagai berikut: Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron.

Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. Elektron terakhir ada pada orbital 3p 1. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron.

Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:.. Elektron terakhir atom x memiliki 4 bilangan. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Konfigurasi elektron menurut bohr adalah sebagai berikut:. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum.

Konfigurasi elektron menurut bohr adalah sebagai berikut: Sehingga konfigurasi elektron dari x −2 adalah: Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24.

Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron.. Nilai keempat bilangan kuantum : Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Konfigurasi elektron dapat dituliskan dengan cara: Unsur 16 x 32 memiliki elektron sebanyak 16, sementara x −2, asalnya dari unsur x yang mendapatkan tambahan 2 buah elektron, sehingga memiliki 16 + 2 = 18 elektron. No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Setiap kulit atom punya maksimum elektron yang dapat ditampung. Elektron terakhir ada pada orbital 3p 1. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi: Elektron terakhir atom x memiliki 4 bilangan.. Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya.

1s 2 2s 2 2p 6 3s 2 3p 6. 13 x = 1s 2 2s 2 2p 6 3s 2 3p 1. 14.06.2020 · tabel konfigurasi elektron lengkap 172 unsur. Ion x +3 memiliki electron = 10 artinya telah melepas 3 elektron. Elektron terakhir ada pada orbital 3p 1. Konfigurasi elektron senyawa x 1s 2 2s 2 2p 6 3s 2 3p 4. Konfigurasi elektron menurut bohr adalah sebagai berikut: Elektron terakhir atom x memiliki 4 bilangan. Konfigurasi elektron dalam atom dapat disusun menurut aturan bohr dan bilangan kuantum. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Maka jumlah electron dari atom x adalah = 10 + 3 = 13 elektron... Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:

Karena yang ditanyakan merupakan anion, berarti kelebihan elektron sehingga perlu ditambah muatannya. Sehingga konfigurasi elektron dari x −2 adalah: Konfigurasi elektron menurut bohr adalah sebagai berikut:. Elektron terakhir atom x memiliki 4 bilangan.

Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah:. Unsur x memiliki nomor atom 33. Konfigurasi elektron menurut bohr adalah sebagai berikut: No.atom x = 16 menangkap elektron 2 ;no.massa = 32. Konfigurasi elektron dapat dituliskan dengan cara: Pada soal, unsur memiliki nomor atom 24, sehingga jumlah elektron unsur tersebut juga 24. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Sehingga konfigurasi elektron dari x −2 adalah:. Keadaaan pada konfigurasi kurang stabil, sehingga perlu mengikuti aturan setengah penuh dan konfigurasi elektronnya menjadi:

Unsur x memiliki nomor atom 33. 1s 2 2s 2 2p 6 3s 2 3p 6. Jumlah elektron maksimum dalam setiap kulit adalah , dengan adalah nomor kulit. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2 n 2, di mana n menunjukkan kulit atom. Unsur x memiliki nomor atom 33. Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: Nilai keempat bilangan kuantum :

Dengan konfigurasi elektron sesuai urutan yang ditunjukkan tanda panah: 1s 2 2s 2 2p 6 3s 2 3p 6.
